DOi:10.13590/j.cjfh.2018.01.011
流动注射法同时检测水中挥发酚和氰化物
(鹿城区疾病预防控制中心,浙江 温州 325000)
收稿日期:2017-12-11
作者简介:┣┣(中)作者简介┫┫张连群 女 检验师 研究方向为理化检验 E-mail:1132593059@qq.com 通信作者:┣┣(中)通信作者┫┫张文珠 女 副主任检验师 研究方向为理化检验 E-mail:958793233@qq.com
基金项目:
摘要:目的 建立连续流动注射分析仪同时测定末梢水中挥发酚和氰化物的分析方法。方法 末梢水经过EDTA和抗坏血酸的混合溶液(20.0 g/L)预处理,用连续流动注射分析仪同时测定挥发酚和氰化物。结果 末梢水样品预处理的条件为50 ml水样中加入0.5 ml EDTA和抗坏血酸的混合溶液(20.0 g/L),加标回收率为90.0%~105.0%,相对标准偏差为0.39%~5.85%,挥发酚和氰化物的检出限分别为0.000 2和0.000 4 mg/L。结论 该方法精密度好,准确度高,符合分析质控要求。
关键词:
流动注射法; 挥发酚; 氰化物; 水; 检测
文章编号:1004-8456(2018)01-0049-05
中图分类号:R155
文献标志码:A
Study on the simultaneous determination of volatile phenol and cyanide in the tap water by flow injection analysis
(Lucheng District Center for Disease Control and Prevention,Zhejiang Wenzhou 325000,China)
Abstract:Objective To establish a flow injection analysis method for simultaneous determination of volatile phenol and cyanide in tap water.Methods The tap water was pretreated by a mixed solution of EDTA and ascorbic acid (20.0 g/L), and the flow injection analyzer was used for simultaneous determination of volatile phenol and cyanide.Results The result show that the mixed solution of EDTA and ascorbic acid (20.0 g/L) of 0.5 ml in 50 ml tap water was the best pretreatment. The recovery rate of the tap water was 90.0%-105.0%, and the relative standard deviation was 0.39%-5.85%. The detection limits of volatile phenol and cyanide were 0.000 2 and 0.000 4 mg/L.Conclusion This method showed good precision, high accuracy, and met the requirements of quality control.
Key words:
Flow injection analysis; volatile phenol; cyanide; water; detection
水中氰化物和挥发酚都属于剧毒物质,长期饮用被其污染的水对人体健康存在着一定的危害,因此准确快速的测定水质样品中的挥发酚和氰化物含量具有非常重要的意义。目前有关利用连续流动注射分析仪测定水中挥发酚或氰化物已有相当多的报道[1-4],与国家标准中传统的检测方法比较显示了较大的优点,比如:分析速度快[5],操作简单[6],准确度和精密度高[5-7],样品和试剂的用量少[5],明显提高了工作效率[5],适合大批量水质样品的分析测定[6,8]等。
本实验室在利用连续流动注射仪对末梢水进行氰化物和挥发酚的同时测定时发现,挥发酚测定的回收率在64.2%~68.1%,氰化物测定的回收率极低,几乎没有,不符合分析质控要求。故本试验就连续流动注射仪同时测定末梢水中挥发酚和氰化物的水质样品进行了预处理条件优化,实现了末梢水中挥发酚和氰化物的同时测定,大大缩短了分析测试时间,试验结果理想。
50%曲拉通溶液TRION X-100(取50 ml曲拉通TRION X-100于100 ml量筒中,加入乙醇至100 ml,混合均匀),蒸馏试剂(取160 ml浓磷酸于适量纯水中,并定容至1 000 ml),储备缓冲液(将9 g硼酸、5 g氢氧化钠和10 g氯化钾溶于纯水中,并定容至1 000 ml),吸收试剂(取100 ml储备缓冲液与1 ml 50%曲拉通溶液混合均匀),氰化物工作缓冲液(取3 g磷酸二氢钾、15 g磷酸氢二钠、3 g二水柠檬酸三钠溶于纯水中并定容到1 000 ml,再加入2 ml 50%曲拉通溶液),氯胺T溶液(取氯胺T 0.2 g溶于纯水中并定容到200 ml),异烟酸溶液[将1.5 g 1-苯基-3-甲基-5-吡唑啉酮完全融入20 ml N,N-二甲基甲酰胺(DMF)溶液,将3.5 g异烟酸和6 ml 5 mol/L氢氧化钠溶于100 ml纯水中,将两种溶液混合,用5 mol/L氢氧化钠或1 mol/L盐酸调节pH值至7.0,定容到200 ml],铁氰化钾溶液(取0.3 g铁氰化钾溶于200 ml储备缓冲液,加入1 ml 50%曲拉通溶液混合均匀),4-氨基安替吡啉溶液(取0.2 g 4-氨基安替吡啉溶于200 ml储备缓冲液,加入1 ml 50%曲拉通溶液,混合均匀),A溶液[20.0 g/L,取2 g 乙二胺四乙酸二钠盐(EDTA)和2 g抗坏血酸溶于纯水中定容到100 ml],B溶液(1 mol/L的氢氧化钠溶液),C溶液(20.0 g/L,2 g硫代硫酸钠溶于100 ml纯水),水中挥发酚标准液[GBW(E)080241,1 000 mg/L(以苯酚计)]、水中氰化物标准液[GBW(E)080115,50.00 μg/ml]均购自中国计量科学研究院。除非另有说明,本试验所用试剂均为分析纯,末梢水取样量均为50 ml。
在同样条件下,测定挥发酚及氰化物混合标准系列溶液的吸光度。试验结果表明,挥发酚在0~0.040 0 mg/L范围内曲线呈良好的线性关系(回归方程y=0.000002x-0.0018,相关系数r=0.999 8);氰化物在0~0.080 0 mg/L范围内也呈现良好的线性关系(回归方程y=0.000002x-0.0010,相关系数r=0.999 8)。
试验结果表明,在水样经过0.5 ml 1 mol/L B溶液预处理后,氰化物测定的回收率没有变化仍为0.0%;经过0.5 ml 20.0 g/L C溶液预处理后,氰化物测定的回收率在86.9%~90.3%;挥发酚测定的基线上漂,测定结果偏高,不满足分析质控要求;而经过0.5 ml 20.0 g/L A溶液预处理过的氰化物测定的回收率明显提高,回收率在92.1%~94.6%之间,已能满足分析质控要求,且挥发酚也显示较好的回收率(96.7%~98.9%),因此,对A溶液中EDTA和抗坏血酸的加入量进行了优化试验,以期找到最经济适宜的加入量,结果见表3。
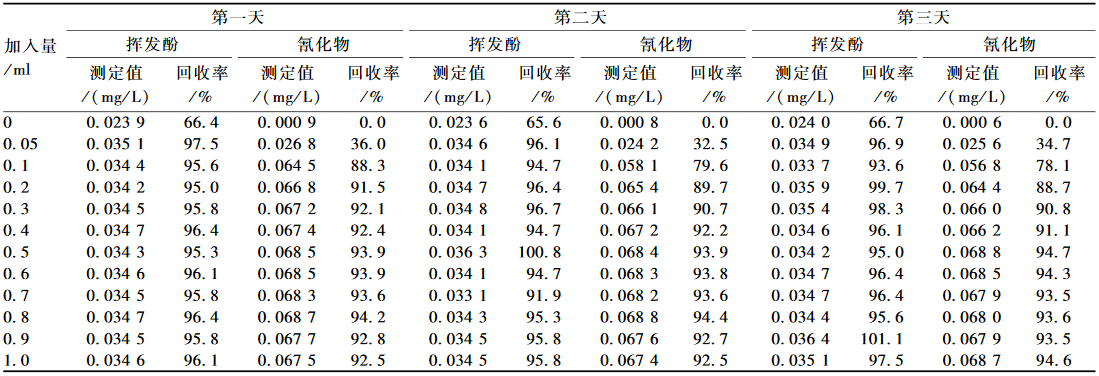
试验结果表明,EDTA和抗坏血酸溶液的加入量为0.3 ml时,氰化物连续3 d测定的回收率均已达90%;当加入量为0.5 ml时,其连续3 d测定的加标回收率分别为93.9%、93.9%和94.7%,随着EDTA和抗坏血酸的继续增加,其回收率变化不大。随着EDTA和抗坏血酸的加入,挥发酚连续3 d测定的回收率分别为95.0%~97.5%、91.9%~100.8%、93.6%~101.1%。结合以上因素,同时从经济角度出发,选择EDTA和抗坏血酸溶液(20.0 g/L)0.5 ml的加入量为最适宜的试验条件。
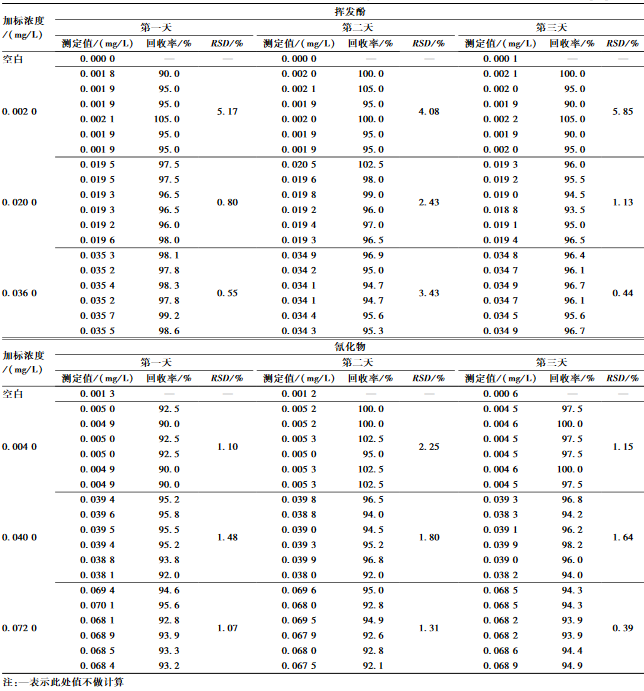
试验结果表明挥发酚连续3 d测定的RSD为0.44%~5.85%,加标回收率在90.0%~105.0%之间;氰化物连续3 d测定的RSD为0.39%~2.25%,加标回收率在90.0%~102.5%之间,表明该条件下同时测定挥发酚和氰化物的精密度好,准确度高,稳定性好,符合分析质控要求。
本实验室在利用连续流动注射仪对末梢水进行氰化物和挥发酚的同时测定时发现,挥发酚测定的回收率在64.2%~68.1%,氰化物测定的回收率极低,几乎没有,不符合分析质控要求。故本试验就连续流动注射仪同时测定末梢水中挥发酚和氰化物的水质样品进行了预处理条件优化,实现了末梢水中挥发酚和氰化物的同时测定,大大缩短了分析测试时间,试验结果理想。
1材料与方法
1.1主要仪器与试剂
AA1连续流动注射分析仪(德国SEAL),氰化物、挥发酚分析模块。50%曲拉通溶液TRION X-100(取50 ml曲拉通TRION X-100于100 ml量筒中,加入乙醇至100 ml,混合均匀),蒸馏试剂(取160 ml浓磷酸于适量纯水中,并定容至1 000 ml),储备缓冲液(将9 g硼酸、5 g氢氧化钠和10 g氯化钾溶于纯水中,并定容至1 000 ml),吸收试剂(取100 ml储备缓冲液与1 ml 50%曲拉通溶液混合均匀),氰化物工作缓冲液(取3 g磷酸二氢钾、15 g磷酸氢二钠、3 g二水柠檬酸三钠溶于纯水中并定容到1 000 ml,再加入2 ml 50%曲拉通溶液),氯胺T溶液(取氯胺T 0.2 g溶于纯水中并定容到200 ml),异烟酸溶液[将1.5 g 1-苯基-3-甲基-5-吡唑啉酮完全融入20 ml N,N-二甲基甲酰胺(DMF)溶液,将3.5 g异烟酸和6 ml 5 mol/L氢氧化钠溶于100 ml纯水中,将两种溶液混合,用5 mol/L氢氧化钠或1 mol/L盐酸调节pH值至7.0,定容到200 ml],铁氰化钾溶液(取0.3 g铁氰化钾溶于200 ml储备缓冲液,加入1 ml 50%曲拉通溶液混合均匀),4-氨基安替吡啉溶液(取0.2 g 4-氨基安替吡啉溶于200 ml储备缓冲液,加入1 ml 50%曲拉通溶液,混合均匀),A溶液[20.0 g/L,取2 g 乙二胺四乙酸二钠盐(EDTA)和2 g抗坏血酸溶于纯水中定容到100 ml],B溶液(1 mol/L的氢氧化钠溶液),C溶液(20.0 g/L,2 g硫代硫酸钠溶于100 ml纯水),水中挥发酚标准液[GBW(E)080241,1 000 mg/L(以苯酚计)]、水中氰化物标准液[GBW(E)080115,50.00 μg/ml]均购自中国计量科学研究院。除非另有说明,本试验所用试剂均为分析纯,末梢水取样量均为50 ml。
1.2方法
1.2.1标准溶液的配制
参照GB/T 5750.4—2006《生活饮用水标准检验方法 感官性状和物理指标》[9]和GB/T 5750.5—2006《生活饮用水标准检验方法 无机非金属指标》[10]确定标准曲线点,将挥发酚和氰化物的标准溶液配制成混合标准使用液(其中挥发酚的浓度为1.00 mg/L,氰化物的浓度为2.00 mg/L)。吸取混合标准溶液0、0.10、0.20、0.40、0.60、0.80、1.00、1.50、2.00 ml于50 ml的容量瓶中,用蒸馏水定容,使挥发酚和氰化物的标准曲线浓度分别为0、0.002 0、0.004 0、0.008 0、0.012 0、0.016 0、0.020 0、0.030 0、0.040 0 mg/L和0、0.004 0、0.008 0、0.016 0、0.024 0、0.032 0、0.040 0、0.060 0、0.080 0 mg/L的混合标准系列溶液。
1.2.2测定
按照仪器操作规程依次开循环冷却水机、流动注射分析仪主机、进样器,打开工作站,待蒸馏器温度升至100 ℃时,打开蠕动泵,激活分析方法,观察气泡形状,调整基线,稳定后,选择合适的增益值,选择编好的运行程序,启动运行分析,仪器自动取样和数据处理。
2结果
2.1检出限、标准曲线
在试验条件下,根据仪器操作规程选择检出限测定组对空白液进行12次测定,计算检出限,其中挥发酚为0.000 2 mg/L,氰化物为0.000 4 mg/L,低于国家标准中传统的检测方法的检出限(0.002 mg/L)[9]。在同样条件下,测定挥发酚及氰化物混合标准系列溶液的吸光度。试验结果表明,挥发酚在0~0.040 0 mg/L范围内曲线呈良好的线性关系(回归方程y=0.000002x-0.0018,相关系数r=0.999 8);氰化物在0~0.080 0 mg/L范围内也呈现良好的线性关系(回归方程y=0.000002x-0.0010,相关系数r=0.999 8)。
2.2末梢水和蒸馏水的测定
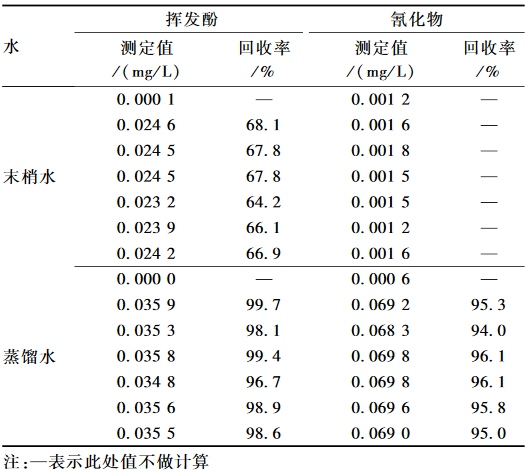
对末梢水和蒸馏水进行空白和加标试验(加标浓度为挥发酚0.036 0 mg/L,氰化物0.072 0 mg/L),每份加标样品各做6个平行试验,结果见表1。由此可见,在蒸馏水中,挥发酚和氰化物均得到了较好的回收率,挥发酚测定的回收率在96.7%~99.7%;氰化物测定的回收率在94.0%~96.1%。而在末梢水中,挥发酚测定的回收率在64.2%~68.1%,氰化物测定的回收率极低,几乎没有,不符合分析质控要求。有可能是末梢水中的游离余氯、金属杂质等对试验有干扰。
|
表1末梢水和蒸馏水中的氰化物和挥发酚测定结果(n=6) Table 1Results of cyanide and volatile phenols in tap water and distilled water |
2.3末梢水预处理条件优化
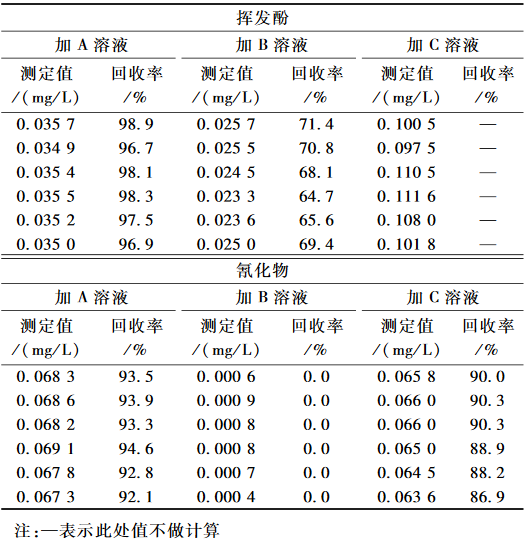
鉴于用连续流动注射仪同时测定末梢水中挥发酚和氰化物时,发现挥发酚和氰化物的加标回收率低下,考虑有可能是末梢水中的游离余氯、金属杂质等对试验有干扰。参照国家标准中水样预处理方法[9],对末梢水进行了预处理,分别加入0.5 ml 20.0 g/L A溶液、0.5 ml 1 mol/L B溶液、0.5 ml 20.0 g/L C溶液,定容至50 ml,加标浓度分别为挥发酚0.036 0 mg/L、氰化物0.072 0 mg/L,各进行6个平行试验,结果见表2。试验结果表明,在水样经过0.5 ml 1 mol/L B溶液预处理后,氰化物测定的回收率没有变化仍为0.0%;经过0.5 ml 20.0 g/L C溶液预处理后,氰化物测定的回收率在86.9%~90.3%;挥发酚测定的基线上漂,测定结果偏高,不满足分析质控要求;而经过0.5 ml 20.0 g/L A溶液预处理过的氰化物测定的回收率明显提高,回收率在92.1%~94.6%之间,已能满足分析质控要求,且挥发酚也显示较好的回收率(96.7%~98.9%),因此,对A溶液中EDTA和抗坏血酸的加入量进行了优化试验,以期找到最经济适宜的加入量,结果见表3。
|
表2预处理后末梢水中挥发酚和氰化物测定结果(n=6) Table 2Results of volatile phenols and cyanide in prepared water |
2.4方法的精密度、准确度和稳定性试验
本试验以相对标准偏差(RSD)来表示精密度,以加标回收率来表示准确度,以连续3 d测定结果的RSD来表示稳定性。取同一末梢水各加入0.5 ml的EDTA和抗坏血酸的混合溶液(20.0 g/L)后,再分别加入低、中、高3种浓度[11]的挥发酚和氰化物的混合标准溶液,按照仪器条件同时测定末梢水中的挥发酚和氰化物,3种浓度各配制6个平行样品,连续测定3 d,结果见表4。
|
表3末梢水中加入不同浓度EDTA和抗坏血酸的混合溶液试验结果 Table 3Experimental results of tap water by pretreated with different concentrations of the mixed solution of EDTA and ascorbic acid |
|
表4低、中、高3种浓度平行测定相对标准偏差和加标回收测定结果(n=6) Table 4Determination results of relative standard deviation and recovery of standard deviation of low, medium and high grade |
3小结
以0.5 ml的EDTA和抗坏血酸的混合溶液(20.0 g/L)预处理末梢水,较经济适宜,利用连续流动注射仪同时测定末梢水中的挥发酚和氰化物的含量,检测分析自动化程度高,操作简单,精密度好,准确度高,稳定性好,符合分析质控要求。另外,末梢水经过预处理后可同时测定挥发酚和氰化物,完成30份样品的测定仅需1 h,大大缩短了分析时间,也减少了取样量,适用于大批量样品的分析检测。
参考文献
[1]刘茂青. 连续流动注射法测定水中挥发酚的含量[J]. 广州化工,2011,39(14):124-125.
[2]汪曼. 连续流动分析仪测定水中氰化物影响因素的研究[J]. 广东化工,2014,41(11):221,216.
[3]郭少维,姜鑫. 流动注射法测定水中挥发酚的研究[J]. 环境保护与循环经济,2011,31(10):40-42.
[4]徐燕. 流动注射分析水中挥发酚、氰化物及阴离子合成洗涤剂[J]. 预防医学论坛,2014,20(6):437-439.
[5]覃苑,唐丽,陈志明,等. 连续流动注射法快速测定废水中挥发酚[J]. 大众科技,2015,17(10):33-34.
[6]鲁莉,杨超,吕晓静. 饮用水中挥发酚、氰化物的流动注射分析[J]. 中国卫生检验杂志,2015,25(15):2474-2476.
[7]罗建民,张静,殷新. 流动注射-在线蒸馏法同时测定水样中挥发酚及氰化物[J]. 光谱实验室,2013,30(5):2525-2528.
[8]诸玉辉. 分光光度法和连续流动分析仪法测定水中氰化物的方法比较[J]. 广东化工,2016,43(22):150-151.
[9]中华人民共和国卫生部,中国国家标准化管理委员会. 生活饮用水标准检验方法 感官性状和物理指标:GB/T 5750.4—2006[S]. 北京:中国标准出版社,2006.
[10]中华人民共和国卫生部,中国国家标准化管理委员会.生活饮用水标准检验方法 无机非金属指标:GB/T 5750.5—2006[S]. 北京:中国标准出版社,2006.
[11]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会. 实验室质量控制规范 食品理化检测:GB/T 27404—2008 [S]. 北京:中国标准出版社,2008.
[2]汪曼. 连续流动分析仪测定水中氰化物影响因素的研究[J]. 广东化工,2014,41(11):221,216.
[3]郭少维,姜鑫. 流动注射法测定水中挥发酚的研究[J]. 环境保护与循环经济,2011,31(10):40-42.
[4]徐燕. 流动注射分析水中挥发酚、氰化物及阴离子合成洗涤剂[J]. 预防医学论坛,2014,20(6):437-439.
[5]覃苑,唐丽,陈志明,等. 连续流动注射法快速测定废水中挥发酚[J]. 大众科技,2015,17(10):33-34.
[6]鲁莉,杨超,吕晓静. 饮用水中挥发酚、氰化物的流动注射分析[J]. 中国卫生检验杂志,2015,25(15):2474-2476.
[7]罗建民,张静,殷新. 流动注射-在线蒸馏法同时测定水样中挥发酚及氰化物[J]. 光谱实验室,2013,30(5):2525-2528.
[8]诸玉辉. 分光光度法和连续流动分析仪法测定水中氰化物的方法比较[J]. 广东化工,2016,43(22):150-151.
[9]中华人民共和国卫生部,中国国家标准化管理委员会. 生活饮用水标准检验方法 感官性状和物理指标:GB/T 5750.4—2006[S]. 北京:中国标准出版社,2006.
[10]中华人民共和国卫生部,中国国家标准化管理委员会.生活饮用水标准检验方法 无机非金属指标:GB/T 5750.5—2006[S]. 北京:中国标准出版社,2006.
[11]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会. 实验室质量控制规范 食品理化检测:GB/T 27404—2008 [S]. 北京:中国标准出版社,2008.
 张连群,张文珠,何纯定.流动注射法同时检测水中挥发酚和氰化物[J].中国食品卫生杂志,2018,30(1):49-53.
张连群,张文珠,何纯定.流动注射法同时检测水中挥发酚和氰化物[J].中国食品卫生杂志,2018,30(1):49-53.