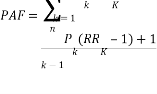我国膳食无机砷致癌症及心血管疾病的疾病模型构建*
李依玲1[ ],刘佳琳1,黄娇2,王彝白纳3,魏晟1
1.华中科技大学同济医学院公共卫生学院流行病与卫生统计学系,湖北 武汉 430030;2. 武汉大学中南医院循证与转化医学中心,湖北 武汉 430071;3.国家食品安全风险评估中心卫生部食品安全风险评估重点实验室,北京 100022
摘要:目的 构建我国膳食无机砷致癌症及心血管疾病的疾病模型。 方法 首先通过检索文献确立膳食无机砷导致的不同健康危害终点。根据我国人群相关疾病的流行病学数据,分别采用风险评估法和反事实分析法计算膳食无机砷暴露致癌症及心血管疾病的归因发病率、死亡率,结合疾病的伤残权重及病程等特点,构建膳食无机砷暴露致癌症及心血管疾病的疾病模型。 结果 人群终身持续经膳食暴露于1μg /(kg·d)无机砷时,引起皮肤癌、膀胱癌和肺癌的概率分别为0.150%、0.014%以及0.170%。我国居民由日常膳食砷暴露[0.46μg /(kg·d)]引起的心血管疾病发病率及死亡率分别为0.039%、0.012%。根据归因发病率和死亡率构建了我国膳食无机砷的疾病模型。 结论 疾病模型可用于计算食品污染物导致的疾病负担,对食品污染物的健康危害进行量化。
关键词 食品污染;无机砷;疾病模型
Construction of disease models for cancer and cardiovascular disease induced by dietary inorganic arsenic in China
LI Yiling1, LIU Jialin1, HUANG Jiao2, WANG Yibaina3, WEI Sheng1
1Department of Epidemiology and Biostatistics, School of Public Health, Tongji Medical College, Huazhong University of Science and Technology, Wuhan 430030, China. 2Center for Evidence-Based and Translational Medicine, Zhongnan Hospital of Wuhan University, Wuhan 430071, China. 3National Food Safety Risk Assessment Center, Key Laboratory of Food Safety Risk Assessment, Ministry of Health, Beijing 100022, China.
Abstract: Objective To construct disease models of dietary inorganic arsenic-induced cancer and cardiovascular disease in China. Methods First, a literature search was conducted to establish different health hazard endpoints due to dietary inorganic arsenic. Based on the epidemiological data of related diseases in the Chinese population, the risk assessment method and counterfactual analysis method were used to calculate the attributable morbidity and mortality of cancer and cardiovascular disease caused by dietary inorganic arsenic exposure. Combined with disability weight and disease course characteristics, a disease model of cancer and cardiovascular disease caused by dietary inorganic arsenic exposure was established. Results The incidence rates of skin cancer, bladder cancer, and lung cancer were 0.150%, 0.014%, and 0.170%, respectively, in Chinese residents exposed to 1μg/(kg·d) inorganic arsenic. The incidence and mortality of cardiovascular diseases caused by daily arsenic exposure [0.46μg/(kg·d)] were 0.039% and 0.012%, respectively. Dietary inorganic arsenic disease models in China were established based on attributable morbidity and mortality. Conclusion The disease model can be used to calculate the burden of disease caused by food contaminants and quantify the health hazards caused by food contaminants.
Key Words Food contamination; Inorganic arsenic; Disease model
砷(Arsenic,As)是一种非金属元素,在自然界中含量丰富,用途广泛。一般人群接触砷的主要途径是摄入被砷污染的食物或水[1]。随着我国对饮水中砷的有效控制[2,3],膳食砷暴露受到越来越广泛的关注,成为人类摄入砷的重要途径[4,5]。砷可分为无机砷(Inorganic Arsenic,iAs)和有机砷(Organic Arsenic),通常无机砷的毒性高于有机砷,更能威胁人类健康[6,7]。1973年,砷及其化合物被国际癌症机构(International Agency for Research on Cancer, IARC)认定为I级致癌物。人体内的砷通过食物链不断积累,可对人体造成一系列健康问题,包括癌症、心血管疾病、神经毒性等[8]。
2006年,WHO成立了食源性疾病负担流行病学工作小组(Foodborne Disease Burden Epidemiology Reference Group, FERG),对食源性疾病的发病率、死亡率和疾病负担进行评估[9]。2012年,FERG建立计算工作组(Computational Task Force, CTF),利用基于危害和归因工作组产生的流行病学信息计算食源性疾病负担[10]。CTF工作流程的起点是构建各种危险因素的疾病模型,以及根据流行病学数据使模型参数化。疾病模型是由与疾病负担原因相关的不同健康状态,以及这些状态之间可能的转换关系构成的示意图[11]。为量化食源性无机砷暴露导致的健康效应,本研究通过查阅文献,首先确立了膳食无机砷导致的不同健康危害终点,结合我国人群相关疾病的流行病学数据构建了膳食无机砷致癌症及心血管疾病的疾病模型框架,为进一步评估膳食无机砷导致的疾病负担提供依据。
1 材料与方法
1.1 确定膳食iAs导致的不同健康危害终点
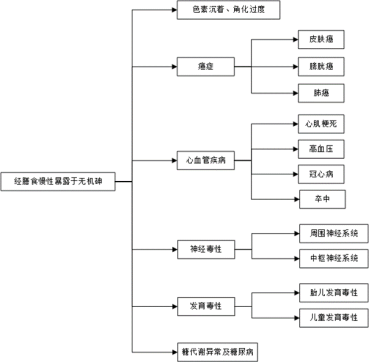
通过系统搜集我国疾病登记系统、专题研究报告等健康相关文献库以及EPA、WHO、EFSA等关于砷的健康危害报告,确定膳食无机砷导致的健康结局主要有皮肤损伤、癌症、心血管疾病、神经毒性、发育毒性、糖代谢异常及糖尿病等,具体如图1所示。考虑到癌症及心血管疾病是砷暴露最常见及最严重的健康效应,国内外相关研究较多,可获得的流行病学数据较全面,故本研究重点关注癌症和心血管疾病这两类健康效应,分别构建膳食无机砷致癌症及心血管疾病的疾病模型。
图1 经膳食慢性暴露于无机砷导致的健康结局
Figure 1 Health outcomes from chronic dietary exposure to inorganic arsenic
构建膳食无机砷疾病模型的关键在于计算膳食无机砷暴露致癌症及心血管疾病的发病率及死亡率,根据FERG的推荐,一般有三种方法可用于计算疾病归因于某特定危险因素的的发生率、死亡率,即分类归因法、比较风险评估法(反事实分析法)和风险评估法[11],结合我国人群膳食无机砷暴露量以及癌症及心血管疾病的总发病率、死亡率等数据,本研究分别采用风险评估法及反事实分析法计算膳食无机砷暴露致癌症及心血管疾病的发病率、死亡率。
1.2.1 膳食iAs暴露致癌症的发病率、死亡率
根据砷致癌症的健康效应,本研究以皮肤癌、膀胱癌和肺癌作为效应终点,采用风险评估法分别计算归因发病率及死亡率。常用的是基于健康指导值(Health-Based Guidance Value,HBGV)的低剂量斜率因子(Slope Factor,SF)外推法。SF(单位为[mg/(kg·d)]-1)指动物或人群终身持续暴露于一个单位浓度[即1mg/(kg·d)]的污染物时,终身超额致癌的风险[12]。本研究基于现有流行病学研究的meta回归分析计算膳食无机砷暴露致肺癌及膀胱癌的SF值,即根据meta回归分析中得到的关于膳食无机砷暴露和肺癌、膀胱癌的研究特异性系数![]() ,再通过以下公式得到我国人群经膳食无机砷暴露引起肺癌、膀胱癌的SF值[13]。具体计算公式如下:
,再通过以下公式得到我国人群经膳食无机砷暴露引起肺癌、膀胱癌的SF值[13]。具体计算公式如下:
(1) |
式中,IR表示研究人群终身患癌累积发病率,![]() 表示 meta回归分析得到的系数,W表示研究人群的平均体重,Q表示人群平均每天对该物质的消费量。
表示 meta回归分析得到的系数,W表示研究人群的平均体重,Q表示人群平均每天对该物质的消费量。
膳食无机砷暴露致皮肤癌的SF值采用国内外研究公认及共同采用的EPA的SF值,为0.0015[μg/(kg·d)]-1[12]。
1.2.2 膳食iAs暴露致心血管疾病的发病率、死亡率
根据可用的流行病学数据,本研究以冠心病、卒中和心血管疾病为健康终点,采用反事实分析法计算膳食无机砷暴露致冠心病、卒中和心血管疾病的发病率、死亡率。其统计基础是人群归因分值(Population Attribution Fraction,PAF),即危险因素暴露水平减至理论最低暴露水平时, 相关疾病发生或死亡减少的百分比[14]。PAF的计算公式如下:
(2) |
式中,n为人群化学物的不同暴露水平,P为暴露水平为n时人群的分布比例,RR为当暴露在水平n时,疾病发病或死亡的相对危险度(Relative Risk, RR)。获得人群归因分值(PAF)后,健康结局归因于危险因素的发病率、死亡率可用以下公式进行计算:
AB=PAF×B | (3) |
式中,AB表示归因于危险因素的发病率、死亡率;PAF表示人群归因危险度;B表示某健康结局的发病率、死亡率。
1.3 构建膳食iAs致癌症及心血管疾病的疾病模型
根据膳食无机砷暴露致癌症及心血管疾病的发病率、死亡率,结合疾病的伤残权重及病程等特点,可构建膳食无机砷暴露致癌症及心血管疾病的疾病模型。
2 结果
2.1 膳食iAs暴露致癌症的疾病模型
由于砷和癌症风险的流行病学证据多来自于饮水砷[13],膳食砷暴露与癌症风险的研究较少,故本研究中,根据我国居民每日的饮水量为1.85L[15],将饮水砷浓度与癌症风险的关系转换为每日砷暴露量与癌症风险的关系,即计算SF值,得到人群终身持续经膳食暴露于1μg /(kg·d)的无机砷时,导致癌症的概率,用以构建经膳食慢性暴露于无机砷导致癌症的疾病模型。
根据《2019中国肿瘤登记年报》[16]中,2017年我国人群膀胱癌和肺癌的终身患癌累积发病率分别为0.39%和4.41%,meta回归分析中得到的无机砷暴露与膀胱癌、肺癌的研究特异性系数![]() 分别为0.0011和0.0012[13],我国成人体重为60kg,饮水摄入量为1.85L,利用公式(1)可计算出膀胱癌和肺癌的SF值分别为0.0001392[μg/(kg·d)]-1和0.0017174[μg/(kg·d)]-1,皮肤癌的SF参考美国环境保护局的综合风险信息系统数据库,为0.0015[μg/(kg·d)]-1[12],表示人群终身持续经膳食暴露于1μg /(kg·d)无机砷时,引起皮肤癌、膀胱癌和肺癌的概率分别为0.15%、0.014%以及0.17%。
分别为0.0011和0.0012[13],我国成人体重为60kg,饮水摄入量为1.85L,利用公式(1)可计算出膀胱癌和肺癌的SF值分别为0.0001392[μg/(kg·d)]-1和0.0017174[μg/(kg·d)]-1,皮肤癌的SF参考美国环境保护局的综合风险信息系统数据库,为0.0015[μg/(kg·d)]-1[12],表示人群终身持续经膳食暴露于1μg /(kg·d)无机砷时,引起皮肤癌、膀胱癌和肺癌的概率分别为0.15%、0.014%以及0.17%。
2.1.2 膳食iAs暴露致癌症的疾病模型
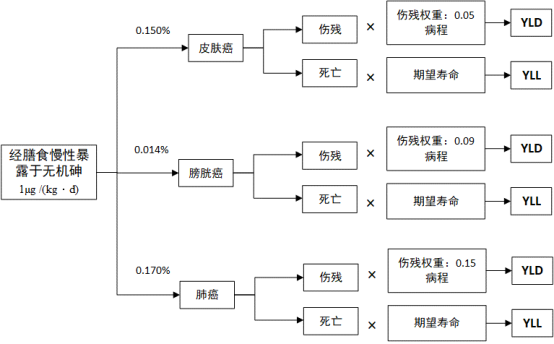
基于经膳食暴露于无机砷致皮肤癌、膀胱癌及肺癌的发病率,结合各类癌症的伤残权重、病程等,可构建经膳食慢性暴露于无机砷导致癌症的疾病模型,如图2所示。
图2 经膳食慢性暴露于无机砷导致癌症的疾病模型
Figure 2 A disease model of cancer induced by chronic dietary exposure to inorganic arsenic
注:YLL (Years of Life Lost),早死所致的寿命损失;YLD (Years Lived with Disability),伤残引起的健康寿命损失年
2.2 膳食iAs暴露致心血管疾病的疾病模型
2.2.1 膳食iAs暴露致心血管疾病的发病率、死亡率
检索文献库中的meta分析研究,以了解iAs暴露与心血管疾病结局之间的剂量-反应关系。由于到目前为止,尚无关于膳食中iAs暴露与心血管疾病风险之间的剂量反应关系的研究报道,因此,参考了一项饮用水中iAs暴露对心血管疾病的相对风险(RRs)的研究[17],该研究包含全球40多万受试者,共包含12项前瞻性研究。该研究表明,饮用水中iAs浓度与心血管疾病的发病率和死亡率有显著相关性,不同饮用水砷暴露水平导致心血管疾病发病率和死亡率的相对风险值RR如表1所示。
表1 与水砷浓度相关的心血管疾病、冠心病和脑卒中的相对风险值[17]
Table 1 Relative risks of cardiovascular disease, coronary heart disease and stroke related to water arsenic concentration
饮用水砷浓度 | CVD发病率 | CVD死亡率 | CHD发病率 | CHD死亡率 | 卒中发病率 | 卒中死亡率 |
10µg/L | 1.00 | 1.00 | 1.00 | 1.00 | 1.00 | 1.00 |
20µg/L | 1.09 | 1.07 | 1.11 | 1.16 | 1.08 | 1.06 |
50µg/L | 1.21 | 1.17 | 1.27 | 1.41 | 1.20 | 1.14 |
100µg/L | 1.32 | 1.25 | 1.40 | 1.64 | 1.29 | 1.21 |
200µg/L | 1.43 | 1.34 | 1.55 | 1.90 | 1.40 | 1.28 |
注:CVD (Cardiovascular Disease),心血管疾病;CHD (Coronary Heart Disease),冠心病
根据该meta分析中得到的CVD的相对风险值与水砷浓度呈对数线性剂量-反应关系,利用表1中结果构建CVD的RR值与水砷对数浓度之间的线性剂量-反应关系模型,如下所示:
RRCVD发病率= 0.1431lnCwater + 0.6628 (4)
RRCVD死亡率 = 0.1130lnCwater + 0.7340 (5)
RRCHD发病率= 0.1826lnCwater + 0.5680 (6)
RRCHD死亡率= 0.2992lnCwater+ 0.2783 (7)
RRstroke发病率=0.1327lnCwater+0.6866 (8)
RRstroke死亡率=0.0933lnCwater+0.7814 (9)
其中Cwater是转化后的无机砷浓度,RRCVD发病率、RRCVD死亡率、RRCHD发病率、RRCHD死亡率、RRstroke发病率、RRstroke死亡率分别是膳食无机砷与心血管疾病、冠心病以及卒中发病与死亡之间的相对危险度。
根据我国成人的饮水量为1.85L/d,我国居民的膳食iAs暴露量来源于第五次中国总膳食研究[18],为27.7μg/d [以成人平均体重60kg计算,为0.46μg /(kg·d)],将膳食iAs暴露量等价转换为饮水砷浓度,再取对数后带入上式中,可得到膳食iAs暴露导致心血管疾病的发病率和死亡率的相对危险度RR值,利用公式(2)可计算相应的PAF值,结果如表2所示。
表2 膳食无机砷暴露导致心血管疾病、冠心病和脑卒中的相对风险值及PAF
Table 2 Relative risks and PAFs of cardiovascular disease, coronary heart disease and stroke due to dietary inorganic arsenic exposure
无机砷暴露量 | 指标 | CVD 发病率 | CVD 死亡率 | CHD 发病率 | CHD 死亡率 | 卒中 发病率 | 卒中 死亡率 |
27.7μg/d | RR | 1.050 | 1.040 | 1.062 | 1.088 | 1.046 | 1.034 |
PAF(%) | 4.768 | 3.828 | 5.852 | 8.089 | 4.372 | 3.278 |
注:CVD (Cardiovascular Disease),心血管疾病;CHD (Coronary Heart Disease),冠心病
根据全球疾病负担(Global Burden of Disease)2017[19]的研究结果,我国2017年冠心病、卒中以及心血管疾病的发病率分别为0.231%、0.257%以及0.816%,死亡率分别为0.126%、0.148%以及0.310%。由公式(3),可计算出膳食砷暴露导致心血管疾病的发病率及死亡率如表3所示。
Table 3 Morbidities and mortalities of cardiovascular diseases due to dietary arsenic exposure
冠心病 | 卒中 | 心血管疾病 | |
发病率 | 0.231% | 0.257% | 0.816% |
5.852% | 4.372% | 4.768% | |
发病率膳食As | 0.014% | 0.011% | 0.039% |
死亡率 | 0.126% | 0.148% | 0.310% |
PAF死亡率 | 8.089% | 3.278% | 3.828% |
死亡率膳食As | 0.010% | 0.005% | 0.012% |
注:PAF发病率、PAF死亡率分别为膳食砷暴露导致心血管疾病发病率及死亡率的人群归因分值,发病率膳食As、死亡率膳食As分别为膳食砷暴露导致心血管疾病发病率及死亡率。
2.2.2 膳食iAs暴露致心血管疾病的疾病模型
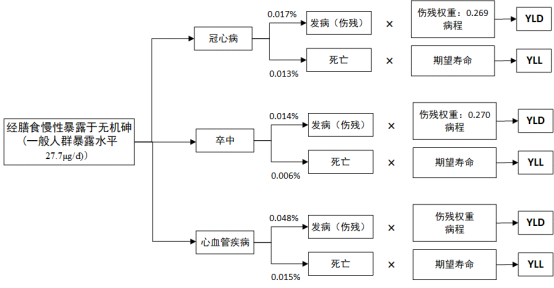
基于表3的结果,可构建经膳食慢性暴露于无机砷导致心血管疾病的疾病模型,如图3所示。
图3 经膳食慢性暴露于无机砷导致心血管疾病的疾病模型
Figure 3 A disease model of cardiovascular disease induced by chronic dietary exposure to inorganic arsenic
注:YLL (Years of Life Lost),早死所致的寿命损失;YLD (Years Lived with Disability),伤残引起的健康寿命损失年
3 讨论
本研究主要参照WHO成立的食源性疾病负担流行病学工作小组(FERG)中疾病模型的构建方法,计算了膳食无机砷导致癌症及心血管疾病的归因发病率、死亡率,构建了膳食无机砷的计算性疾病模型。计算性疾病模型是以危害为出发点,采用图解的形式,展示与食源性危害因素相关的各种健康结局,包括急性、慢性后遗症和死亡等,以及这些结局之间可能的转换概率,是对疾病生物学转归过程、流行病学数据可用性和参数估计三方面信息的综合。计算性疾病模型的构建可为食源性疾病负担的评估提供思路和所需要的参数,基于疾病模型,可评估食品污染物导致的疾病负担,量化其造成的健康效应。本研究基于WHO疾病模型建立的基本方案和数据驱动原则,结合我国数据特点,建立了我国的一种污染物暴露与多种健康结局的疾病模型和各节点转归参数计算方法。以食品污染物无机砷为例,构建了膳食砷暴露导致癌症及心血管疾病的疾病模型。
本研究为构建一种食品污染物暴露与多种健康结局的疾病模型提供了思路,疾病模型的构建可用于计算食品污染物导致的疾病负担,对食品污染物的健康危害进行量化,从而为相关部门制定政策和策略提供依据。
参考文献
[1] IARC. Arsenic, Metals, Fibres, and Dusts, Vol. 100 C: A Review of Human Carcinogens[M]. Geneva: WHO Press, 2012.
[2] 仝璐, 夏雅娟. 改水干预对饮水型地方性砷中毒健康效应影响的研究进展[J]. 疾病监测与控制, 2018, 12(02): 144-148+152.
[3] 张秋秋, 潘申龄, 刘伟, 等. 我国重点城市饮用水中砷健康累积风险评价[J]. 环境科学, 2017, 38(05): 1835-1841.
[4] 杨倩琪, 黄蕾, 布文博, 等. 南京市人群膳食砷暴露健康风险研究[J]. 环境卫生学杂志, 2018, 8(03): 191-196.
[5] 袁文婷, 刘宇, 程国霞, 等. 陕西主要食品中砷污染及居民膳食暴露风险评估[J]. 现代预防医学, 2021, 48(01): 55-58.
[6] WHO. Arsenic and Arsenic Compounds (Environmental Health Criteria 224), 2nd ed[M]. Geneva: World Health Organization, International Programme on Chemical Safety, 2001.
[7] GRINHAM A, KVENNEFORS C, FISHER P L, et al. Baseline arsenic levels in marine and terrestrial resources from a pristine environment: Isabel Island, Solomon Islands[J]. Mar Pollut Bull, 2014, 88(1-2): 354-60.
[8] Scientific opinion on arsenic in food[EB/OL]. [2021-12-28]. https://sci⁃hub.tw/10.2903/j.efsa.2009.1351.
[9] KUCHENMüLLER T, HIRD S, STEIN C, et al. Estimating the global burden of foodborne diseases--a collaborative effort[J]. Euro Surveill, 2009, 14(18).
[10] KUCHENMüLLER T, ABELA-RIDDER B, CORRIGAN T, et al. World Health Organization initiative to estimate the global burden of foodborne diseases[J]. Rev Sci Tech, 2013, 32(2): 459-67.
[11] DEVLEESSCHAUWER B, HAAGSMA J A, ANGULO F J, et al. Methodological Framework for World Health Organization Estimates of the Global Burden of Foodborne Disease[J]. PLoS One, 2015, 10(12): e0142498.
[12] Arsenic, inorganic; CASRN 7440⁃38⁃2[EB/OL]. [2021-12-28]. https://cfpub.epa.gov/ncea/iris/iris_documents/documents/subst/0278_summary.pdf#nameddest=canceroral.
[13] LYNCH H N, ZU K, KENNEDY E M, et al. Quantitative assessment of lung and bladder cancer risk and oral exposure to inorganic arsenic: Meta-regression analyses of epidemiological data[J]. Environ Int, 2017, 106: 178-206.
[14] WHO. Comparative quantification of risks[M]. Geneva: World Health Organization, 2004.
[15] 环境保护部. 中国人群暴露参数手册(成人卷)[M]. 北京: 中国环境出版社, 2013.
[16] 郝捷, 魏文强. 2019中国肿瘤登记年报[M]. 北京: 人民卫生出版社, 2021.
[17] MOON K A, OBEROI S, BARCHOWSKY A, et al. A dose-response meta-analysis of chronic arsenic exposure and incident cardiovascular disease[J]. Int J Epidemiol, 2017, 46(6): 1924-1939.
[18] 吴永宁, 赵云峰, 李敬光. 第五次中国总膳食研究[M]. 北京: 科学出版社, 2018.
[19] GBD 2017 Risk Factor Collaborators. Global, regional, and national comparative risk assessment of 84 behavioural, environmental and occupational, and metabolic risks or clusters of risks for 195 countries and territories, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017[J]. Lancet, 2018, 392(10159): 1923-1994.