DOi:10.13590/j.cjfh.2018.01.022
壬基酚每日可耐受摄入量建议值的探讨
(1.四川大学华西公共卫生学院 四川省食品安全监测与风险评估重点实验室,四川 成都 610041; 2.国家食品安全风险评估中心,北京 100022)
收稿日期:2017-10-08
作者简介:陈锦瑶 女 副教授 研究方向为食品安全与风险评估 E-mail:umbrellayy@163.com通信作者:包汇慧 女 副研究员 研究方向为食品化学物风险评估 E-mail: baohuihui@cfsa.net.cn
基金项目:
摘要:目的 对壬基酚的健康指导值进行探讨,为进一步评估壬基酚暴露对人类健康的风险奠定基础。方法 本研究采用系统综述的原则与方法,在广泛检索现有壬基酚毒理学数据的基础上,筛选高质量的文献纳入研究数据库,经全面评估后选择适宜的临界效应,结合不确定性分析确定壬基酚的每日可耐受摄入量。结果 经过文献收集和筛选,最终选用以一项较高质量多代生殖毒性研究中观察到的肾脏毒性为敏感指标,以其观察到有害作用的最低水平(lowest observable adverse effect level,LOAEL)为外推起始点,使用LOAEL-不确定系数法进行推算。结论 壬基酚的每日可耐受摄入量为0.025 mg/kg BW。
关键词:
壬基酚; 食品安全; 风险评估; 每日可耐受摄入量; 食品安全标准
文章编号:1004-8456(2018)01-0104-05
中图分类号:R155
文献标志码:A
Discussion of tolerable daily intake for nonylphenol
((1.Food Safety Monitoring and Risk Assessment Key Laboratory of Sichuan Province, WestChina School of Public Health,Sichuan University, Sichuan Chengdu 610041, China; 2.China National Center for Food Safety Risk Assessment, Beijing 100022, China)
Abstract:Objective To investigate and analyze the epidemiological characteristics of the poisoning incident, identify the poisonous mushroom species, put forward the prevention and control measures, and to explore measures to prevent the recurrence of poisoning incidents.Methods This poisoning event was analyzed by case definition, case search, case interview, recipe survey, field sampling and morphological identification of poisonous mushrooms.Results Five migrant workers picked and ate about 150 g of the wild mushrooms. 8.3-10 hours later, nausea, vomiting, diarrhea, abdominal pain and other gastrointestinal symptoms appeared, and the clinical examination showed liver damage. After 2 days of symptomatic treatment including gastric lavage, plasma exchange, activated carbon absorption, fluid infusion and protecting liver and stomach for clearance of toxic substance, 2 cases were found to have pseudo-recovery period. One day later, these 2 cases had a sharp deterioration. In the next few days all patients progressed to liver failure and died of multiple organ failure, both morbidity and mortality were 100% (5/5). The recipe survey showed that there was no other poisoning food except the mushrooms. The morphological identification result showed it was Amanita rimosa. The food poisoning incident was due to mistaken eating of wild mushrooms collected from park M, and the poisonous mushroom was virulent Amanita rimosa.Conclusion This poisoning incident of mistaken eating of Amanita rimosa was reported in Guangdong Province for the first time. The natural disease history of Amanita rimosa poisoning was described comprehensively in this study. The appearance of these fungi was extremely similar with those of some edible fungi, and was difficult to distinguish them, which cause the mistaken eating very easily. The health education should be further strengthened to remind people not to eat wild mushrooms, and it was the most basic way to prevent mushroom poisoning.
Key words:
Risk communication; food safety standards; media monitoring; news report analysis
壬基酚(nonylphenol,NP)是一种重要的精细化工原料和中间体,广泛应用于增塑剂、表面活性剂、抗氧化剂、纺织印染助剂、农药乳化剂等工业领域。进入环境的NP主要释放入水体(95%),少部分进入土壤(4%)和大气(1%)[1]。作为一种典型的环境内分泌干扰物,NP化学性质稳定,释放入环境后很难被降解,易在污水污泥、流水沉积物中聚集,并通过食物链由低级向高级传递,进而对人体产生危害[2]。食品包装材料中的NP迁移入食物,是食物NP污染的另一重要来源。张庆等[3]进行了塑料食品包装材料的NP迁移评估,结果发现部分含有高浓度NP的食品包装材料对人体健康存在较高风险。
广义上NP包含了大量的同分异构体,主要具有两类变化方式:壬基与苯酚分子连接位置变化及壬基支链结构的变化。工业生产的NP主要是在其烷基上具有不明支链的4-NP(p-NP),而极少出现直链[4]。目前多数研究主要针对4-NP与其下的同分异构体(CAS:84852-15-3),以及无不明支链的NP(CAS:25154-52-3),本次评估也仅针对上述两种物质。
目前已有一些国家和国际组织对NP进行了风险评估[1,4-6],但仅有丹麦在其评估中提出了每日耐受摄入量(tolerable daily intake,TDI)为0.005 mg/kg BW[1]。我国是NP生产和消费大国,国家食品安全风险评估中心和北京市疾病预防控制中心根据总膳食调查数据已陆续开展了中国人NP的暴露量评估[7],但我国目前尚未制定相关健康指导值,因此,本研究通过系统地检索NP的毒理学文献资料和相关数据,根据风险评估的原则和方法,提出了NP的TDI建议值,为其进一步的风险评估和管理提供依据。
在资料分析时首先分析和引用其他国际组织评估和系统综述的结果,其次是人群毒性相关资料,然后为动物试验和体外研究资料。将纳入的毒理学文献根据Klimsch分级标准[8]进行分级。Klimsch分级标准为目前国际上常用的三种毒理学数据评价系统之一,该评价标准根据研究可靠性将其分为四类:第一类为“无限制的可靠类”,即根据现行有效的试验指南和/或国际广泛认可的试验指南,最好遵循良好实验室规范(good laboratory practice,GLP)实施的试验(或方法与其非常接近);第二类为“有限制的可靠类”,即未根据现行指南实施,但试验方法记录充分且具有科学性;第三类为“不可靠类”,即检测方法、受试物、暴露方式等存在局限性,结论不具有说服力;第四类为“无法归属类”,即报告未列出详细信息。最后根据风险评估中危害识别和危害特征描述的原则与方法,对分析结果进行总结归纳,提出TDI建议值。
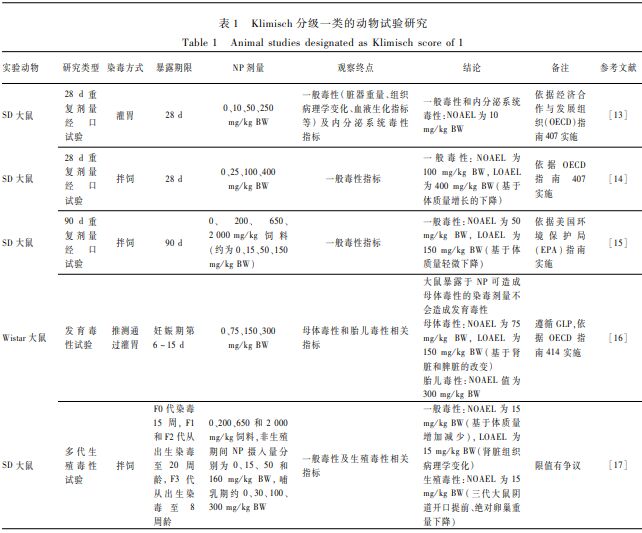
尚未查到可用的关于NP的人体研究资料,故本研究仅分析了动物试验和体外试验资料。纳入动物试验和体外试验研究共84篇,其中中文文献18篇,英文文献66篇。其中可用于制定健康指导值的文献共29篇,根据Klimsch分级标准,第一类毒理学研究有5篇(见表1),第二类12篇,第三类12篇。研究类型包括28 d、60 d毒性和90 d重复剂量毒性试验(两个物种)以及发育毒性试验(两个物种)、两代生殖毒性试验、多代生殖毒性试验、致突变试验等。数据库涵盖了多暴露时长、多物种、多毒理学终点,且至少具有一项可靠的亚慢性毒性研究,满足推导慢性健康指导值所需的条件[9]。
在一项根据OECD指南414实施的标准发育毒性试验中,可引起明显母体毒性(体质量增重降低、摄食量减少)的剂量未见引起发育毒性(着床后丢失,每窝产仔数,胎儿体质量和严重/微小胎儿畸形发生率等均未受影响),该研究所得母体毒性NOAEL为75 mg/kg BW、胎体毒性NOAEL为300 mg/kg BW(试验最高剂量)[16]。另有研究[24]表明围生期暴露于0.1 mg/kg BW NP即可导致子代发生行为学改变。
本次健康指导值推导包含的不确定性主要包括以下几个方面:(1)实验动物外推到人的不确定性(UFA)。因本研究缺乏NP毒代动力学研究数据,无法推断实验动物与人体之间毒代动力学和毒物动力学的差异,因此UFA设定为10。(2)人群中个体敏感性的变异(UFH)。本研究缺乏NP在敏感人群中的剂量-反应关系数据,因此亦沿用默认值10。(3)以LOAEL代替NOAEL时的不确定性(UFL)。由于肾脏损伤的剂量-反应关系曲线在低剂量时较平缓,本研究中将UFL设为3。(4)另有研究提示NP具有发育神经毒性和发育免疫毒性,但相关研究尚不充分,仍存在许多不确定性,无法判定其剂量-反应关系。因此,考虑到NP出生前后暴露可能导致的对发育神经调节和免疫调节的可能影响,且现有资料缺乏/尚不明确带来的不确定性,本研究设定修正系数(MF)为2。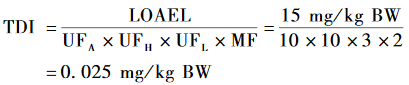
广义上NP包含了大量的同分异构体,主要具有两类变化方式:壬基与苯酚分子连接位置变化及壬基支链结构的变化。工业生产的NP主要是在其烷基上具有不明支链的4-NP(p-NP),而极少出现直链[4]。目前多数研究主要针对4-NP与其下的同分异构体(CAS:84852-15-3),以及无不明支链的NP(CAS:25154-52-3),本次评估也仅针对上述两种物质。
目前已有一些国家和国际组织对NP进行了风险评估[1,4-6],但仅有丹麦在其评估中提出了每日耐受摄入量(tolerable daily intake,TDI)为0.005 mg/kg BW[1]。我国是NP生产和消费大国,国家食品安全风险评估中心和北京市疾病预防控制中心根据总膳食调查数据已陆续开展了中国人NP的暴露量评估[7],但我国目前尚未制定相关健康指导值,因此,本研究通过系统地检索NP的毒理学文献资料和相关数据,根据风险评估的原则和方法,提出了NP的TDI建议值,为其进一步的风险评估和管理提供依据。
1研究方法
对NP毒理学数据进行系统检索,筛选出高质量的文献纳入NP风险评估数据库。依据“nonylphenol”“toxicity”“exposure”“alkylphenols”等关键词在PubMed、CNKI、万方等数据库中进行检索,检索期限均为数据库起始收录日期到2015年12月。纳入标准:NP一般毒性以及生殖发育毒性、内分泌干扰毒性、致突变性、致癌性等特殊毒性的中英文研究;排除标准:非NP单独暴露研究、仅有摘要的研究、相关性不大或重复的研究。在资料分析时首先分析和引用其他国际组织评估和系统综述的结果,其次是人群毒性相关资料,然后为动物试验和体外研究资料。将纳入的毒理学文献根据Klimsch分级标准[8]进行分级。Klimsch分级标准为目前国际上常用的三种毒理学数据评价系统之一,该评价标准根据研究可靠性将其分为四类:第一类为“无限制的可靠类”,即根据现行有效的试验指南和/或国际广泛认可的试验指南,最好遵循良好实验室规范(good laboratory practice,GLP)实施的试验(或方法与其非常接近);第二类为“有限制的可靠类”,即未根据现行指南实施,但试验方法记录充分且具有科学性;第三类为“不可靠类”,即检测方法、受试物、暴露方式等存在局限性,结论不具有说服力;第四类为“无法归属类”,即报告未列出详细信息。最后根据风险评估中危害识别和危害特征描述的原则与方法,对分析结果进行总结归纳,提出TDI建议值。
2结果
2.1文献收集和筛选
目前已有一些国家和国际组织对NP进行了风险评估[1,4-6]。丹麦兽医和食品管理局(Danish Veterinary and Food Administration)在2000年对NP进行的风险评估中以三代动物经口暴露研究观察到的生殖/发育影响为临界效应,以其观察到有害作用的最低水平(lowest observed adverse effect level,LOAEL)15 mg/kg为剂量-反应关系外推的起始点(该剂量也是肾脏效应的LOAEL),不确定系数(uncertainty factors,UFs)为3 000(10×10×30,分别表示实验动物外推到人的不确定性,人群中敏感个体的不确定性,以LOAEL计算和缺乏关于NP的遗传毒性和致癌性数据的不确定性),将NP的TDI定为0.005 mg/kg BW[1]。欧盟2002年对NP的风险评估报告中,以安全范围(MOS)为指标进行危害表征,认为NP引起消费者急性毒性(LD50为1 200~2 400 mg/kg BW)、重复剂量毒性(LOAEL为15 mg/kg BW)和生殖毒性[未观察到有害作用的水平(NOAEL)为15 mg/kg BW]等健康效应的风险很低[4]。尚未查到可用的关于NP的人体研究资料,故本研究仅分析了动物试验和体外试验资料。纳入动物试验和体外试验研究共84篇,其中中文文献18篇,英文文献66篇。其中可用于制定健康指导值的文献共29篇,根据Klimsch分级标准,第一类毒理学研究有5篇(见表1),第二类12篇,第三类12篇。研究类型包括28 d、60 d毒性和90 d重复剂量毒性试验(两个物种)以及发育毒性试验(两个物种)、两代生殖毒性试验、多代生殖毒性试验、致突变试验等。数据库涵盖了多暴露时长、多物种、多毒理学终点,且至少具有一项可靠的亚慢性毒性研究,满足推导慢性健康指导值所需的条件[9]。
2.2危害识别
2.2.1毒代动力学
NP经口暴露的毒代动力学资料较少,大多基于有一定缺陷的大鼠和人体试验。NP通过胃肠道吸收较快,吸收量可能较大。NP主要通过葡糖苷酸和硫酸盐结合途径代谢。有证据表明,NP经胃肠道吸收后可出现较大程度首过效应(经肝脏代谢)。由于存在首过效应的原因,经口暴露的非结合型NP生物利用度有限(不超过给药剂量的10%~20%)。NP可在全身广泛分布,在脂肪中的浓度含量最高。没有足够的数据表明NP是否有潜在的生物蓄积作用。NP主要通过尿液和粪便排泄[10]。
2.2.2急性毒性
尚无人体数据可参考。动物试验表明NP经口暴露毒性较低,其雄性大鼠LD50值为 1 200~2 400 mg/kg BW,雌性为1 600~1 900 mg/kg BW[11-12]。NP致死率的剂量-反应曲线较陡峭[10]。
|
表1Klimisch分级一类的动物试验研究 Table 1Animal studies designated as Klimisch score of 1 |
2.2.3重复剂量毒性
尚无人体数据可参考。欧盟采用一项高质量的经口多代生殖毒性试验结果(拌饲染毒20周),基于该研究中观察到的肾脏组织病理学变化(肾小管变性或扩张),将LOAEL值设为15 mg/kg BW[17]。美国EPA在其报告中也同样采纳了该研究,但EPA采用了体质量下降终点,将LOAEL设为50 mg/kg BW,NOALE为15 mg/kg BW[5]。在最近发表的一项根据OECD指南407实施的28 d经口试验中,50 mg/kg BW剂量下观察到了雄性大鼠甲状腺重量明显增加,雌性大鼠血液生化指标改变,故将NOAEL设为10 mg/kg BW[13]。肝、肾可能是NP经口重复剂量毒性的靶器官。通过灌胃法给药时NP的经口毒性上升,100 mg/kg BW或以上剂量水平开始出现死亡[18]。
2.2.4生殖发育毒性
尚无人体数据可参考。一些试验研究结果表明NP具有雌激素活性,但活性比雌二醇少3~6个数量级[19-23]。一项高质量的经口多代生殖毒性试验结果(拌饲法染毒)显示大鼠多代暴露于NP可轻微扰乱子代生殖系统(发情周期略有变化、阴道开口时间以及还可能存在的卵巢重量和精子/精子细胞计数的改变),该毒性作用可能由NP的雌激素活性引起,其NOAEL为15 mg/kg BW。在后代中观察到的生殖系统扰乱与外源性雌激素活性的预测或假设效应一致[17]。有证据[18]显示NP还具有睾丸毒性(生精小管空泡变性、细胞坏死和小管直径减小),睾丸毒性的LOAEL值为100 mg/kg BW。在一项根据OECD指南414实施的标准发育毒性试验中,可引起明显母体毒性(体质量增重降低、摄食量减少)的剂量未见引起发育毒性(着床后丢失,每窝产仔数,胎儿体质量和严重/微小胎儿畸形发生率等均未受影响),该研究所得母体毒性NOAEL为75 mg/kg BW、胎体毒性NOAEL为300 mg/kg BW(试验最高剂量)[16]。另有研究[24]表明围生期暴露于0.1 mg/kg BW NP即可导致子代发生行为学改变。
2.2.5致突变性
尚无人体数据可参考。NP在细菌回复突变试验[25]和体外哺乳动物细胞基因突变试验[26]中均为阴性结果。两项体内微核试验[27-28]结果为阴性(腹腔注射和经口给药),但其中的经口给药研究存在方法上的缺陷。现有数据提示NP可能没有致突变性。
2.2.6致癌性
尚无人体或动物试验研究数据,但可从其他数据获取相关信息。从现有致突变试验结果看,NP通过遗传毒性机制引发癌症的可能性很低;在标准重复暴露毒性试验中也未观察到持续细胞增殖或增生,故NP通过非遗传毒性机制致癌的可能性也较低[9]。
2.2.7其他特殊毒性
近年的非标准化体内/外试验研究提示,NP可能具有一定的神经毒性及免疫毒性作用,但研究数据尚不足,无法判定其靶标及阈剂量。
2.3危害特征描述
由于本研究拟推导终身暴露的TDI值,而数据库中缺乏高质量的亚慢性/慢性喂养试验,因此有关重复剂量毒性试验的信息由一项高质量(即Klimisch一类)的多代生殖毒性研究提供[17]。欧盟和丹麦的风险评估基于该研究中的肾脏组织病理学变化(肾小管变性和/或扩张发生率增加),设定LOAEL为15 mg/kg BW;美国EPA则是基于大鼠体质量增重减少,将LOAEL设为50 mg/kg BW、NOAEL为15 mg/kg BW;此外,该研究还观察到生殖毒性(三代大鼠阴道开口提前、绝对卵巢重量下降),其NOAEL为15 mg/kg BW,LOAEL为50 mg/kg BW。在该研究中,仅中、高剂量组的实验动物出现生殖毒性相关指标的轻微改变和增重减少,而4个世代的实验动物均在最低剂量组即出现了肾脏组织病理学改变。虽然肾脏损伤效应缺乏统一的剂量依赖性趋势,但该效应为背景变异的可能性很低[10],故本研究中拟采用肾脏损伤效应作为临界效应。目前国际上使用较多的剂量-反应关系外推法有NOAEL/LOAEL法、基准计量法和分类回归法等,但由于使用数学模型拟合需要较为详细的数据,而本次研究选用的试验研究尚有一些数据不明确,故暂不使用基准剂量法推导TDI,因此,本研究选择该试验中观察到的肾脏毒性(肾小管变性和/或扩张)作为临界效应,以其LOAEL(15 mg/kg BW)为剂量-反应外推的起始点,采用LOAEL-不确定系数法来推导TDI值。本次健康指导值推导包含的不确定性主要包括以下几个方面:(1)实验动物外推到人的不确定性(UFA)。因本研究缺乏NP毒代动力学研究数据,无法推断实验动物与人体之间毒代动力学和毒物动力学的差异,因此UFA设定为10。(2)人群中个体敏感性的变异(UFH)。本研究缺乏NP在敏感人群中的剂量-反应关系数据,因此亦沿用默认值10。(3)以LOAEL代替NOAEL时的不确定性(UFL)。由于肾脏损伤的剂量-反应关系曲线在低剂量时较平缓,本研究中将UFL设为3。(4)另有研究提示NP具有发育神经毒性和发育免疫毒性,但相关研究尚不充分,仍存在许多不确定性,无法判定其剂量-反应关系。因此,考虑到NP出生前后暴露可能导致的对发育神经调节和免疫调节的可能影响,且现有资料缺乏/尚不明确带来的不确定性,本研究设定修正系数(MF)为2。
3TDI的确定
综上,根据本研究的结果,并经NP风险评估专家小组讨论决定,以一项较高质量的美国国家毒理学计划(NTP)多代生殖毒性研究[17]中观察到的肾脏毒性(肾小管变性和/或扩张)为最敏感指标,以其LOAEL(15 mg/kg BW)为剂量-反应关系外推的起始点,其中不确定性因素包括实验动物外推到人的不确定性UFA(10)、人群敏感个体的不确定性UFH(10)、LOAEL代替NOAEL时的不确定性UFL(3)和修正系数MF(2)。按照NOAEL/LOAEL-不确定系数法,按下式计算得出NP的TDI值为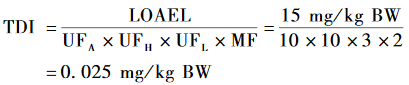
参考文献
[1]NIELSEN E, OSTERGAARD G, THORUP I, et al. Toxicological evaluation and limit values for nonylphenol, nonylphenol ethoxylates, tricresyl, phosphates and benzoic acid[R/OL]. 2000 [2017-09-22]. http://www.statensnet.dk/pligtarkiv/fremvis.pl?vaerkid=6944&reprid=0&filid=22.
[2]SNEDEKER S, HAY A. The alkylphenols nonylphenol and octylphenol in food contact materials and household items: exposure and health risk considerations[M]//SNEDEKER S M. Toxicants in food packaging and household plastics. London: Springer, 2014:125-150.
[3]张庆, 白桦, 马强, 等. 塑料食品包装材料中壬基酚的风险评估[J].食品工业科技, 2011, 32(9):340-343.
[4]European Commission: Joint Research Centre, Institute for Health and Consumer Protection, European Chemicals Bureau. European Union risk assessment report: 4-nonylphenol (branched) and nonylphenol[R]. Luxembourg: Office of Official Journal of the European Communities, 2002.
[5]US Environmental Protection Agency. Screening-level hazard characterization: akylphenols category[R/OL]. 2009 [2017-09-22]. https://www.epa.gov/chemicals-under-tsca.
[6]Canadian Environmental Protection Act, Priority substances list assessment report. Nonylphenol and its ethoxylates[R]. Canada: Environment Canada and Health Canada,1999.
[7]NIU Y M, ZHANG J, DUAN H J, et al. Bisphenol A and nonylphenol in foodstuffs: Chinese dietary exposure from the 2007 total diet study and infant health risk from formulas[J]. Food Chem, 2015,167(6): 320-325.
[8]KLIMISCH H J, ANDREAE M, TILLMANN U. A systematic approach for evaluating the quality of experimental toxicological and ecotoxicological data[J]. Regul Toxicol Pharmacol, 1997, 25(1):1-5.
[9]US Environmental Protection Agency. A review of the reference dose and reference concentration processes[J/OL]. 2013 [2017-09-22]. https://www.epa.gov/osa/basic-information-about-risk-assessment-guidelines-development.
[10]European Commission. European Union risk assessment report (version for TMIII98) [R]. 1998.
[11]BEROL KEMI A B. Nonylphenol acute oral toxicity in rats[R]. Inveresk Research International Project No. 230086, report No. 2379, 1982.
[12]ICI Central Toxicology Laboratory. Nonylphenol (ex-oil Works and Rohm and Haas): comparison of acuteoral toxicities[R]. CTL Report No. CTL/L/708, 1984.
[13]WOO G H, SHIBUTANI M, ICHIKI T, et al. A repeated 28-day oral dose toxicity study of nonylphenol in rats, based on the ‘enhanced OECD test guideline 407’ for screening of endocrine-disrupting chemicals[J].Arch Toxicol, 2007, 81(2):77-88.
[14]HLS A G. Nonylphenol: 28 day oral (dietary) sub-acute toxicity study in the rat[R]. Hazleton UK report no.5917-671/1, 1989.
[15]CUNNY H C, MAYES B A, ROSICA K A, et al. Subchronic toxicity (90-day) study with para-nonylphenol in rats[J]. Reg Toxicol Pharmacol, 1997, 26(2):172-178.
[16]Initiative Umweltrelevante Altstoffe. Teratogenicity study in Wistar rats treated orally with “nonylphenol”[R]. IBR Project No.20-04-0502/00-91, 1992.
[17]NTP. Nonylphenol: multigenerational reproductive effects in Sprague-Dawley rats when exposed to nonylphenol in the diet[R]. R.O.W. Sciences Study No.8989-30, 1997.
[18]DE JAGER C, BORNMAN M S, VAN DER HORST G. The effect of p-nonylphenol, an environmental toxicant with oestrogenic properties, on fertility potential in adult male rats[J]. Andrologia, 1999, 31(2): 99-106.
[19]ROUTLEDGE E J,SUMPTER J P. Structural features of alkylphenolic chemicals associated with estrogenic activity[J]. J Biol Chem,1997, 272(6): 3280-3288.
[20]SOTO A M, JUSTICIA H, WRAY W W, et al. p-Nonyl-phenol: an estrogenic xenobiotic released from “modified” polystyrene[J]. Environ Health Perspect, 1991(92):167-173.
[21]WHITE R, JOBLING S, HOARE S A, et al. Environmentally persistent alkylphenolic compounds are estrogenic[J]. Endocrinology,1994, 135(1):175-182.
[22]ODUM J, LEFEVRE P A, TITTENSOR S, et al. The rodent uterotrophic assay: critical protocol features, studies with nonylphenols, and comparison with a yeast estrogenicity assay[J]. Reg Toxicol Pharmacol,1997, 25(2): 176-188.
[23]LEE P C, LEE W. In vivo estrogenic action of nonylphenol in immature female rats[J]. Bull Environ Contam Toxicol,1996, 57(3): 341-348.
[24]NEGISHI T, KAWASAKI K, SUZAKI S, et al. Behavioral alterations in response to fear-provoking stimuli and tranylcypromine induced by perinatal exposure to bisphenol A and nonylphenol in male rats[J]. Environ Health Perspect, 2004,112(11): 1159-1164.
[25]SHIMIZU H, SUZUKI Y, TAKEMURA N, et al. The results of microbial mutation test for forty-three industrial chemicals[J]. Sangyo Igaku, 1985, 27(6): 400-419.
[26]HLS A G. In vitro mammalian cell gene mutation test with nonylphenol[R]. IBR Project No.95-86-0449-90,1990.
[27]HLS A G. Mutagenittsuntersuchung von nonylphenol im mikrokern-test[R]. Hüls Report Dated 16.08.88, 1988.
[28]HLS A G. In vivo mouse micronucleus test[R]. Hüls Report No. MK-99/0255,1996.
[2]SNEDEKER S, HAY A. The alkylphenols nonylphenol and octylphenol in food contact materials and household items: exposure and health risk considerations[M]//SNEDEKER S M. Toxicants in food packaging and household plastics. London: Springer, 2014:125-150.
[3]张庆, 白桦, 马强, 等. 塑料食品包装材料中壬基酚的风险评估[J].食品工业科技, 2011, 32(9):340-343.
[4]European Commission: Joint Research Centre, Institute for Health and Consumer Protection, European Chemicals Bureau. European Union risk assessment report: 4-nonylphenol (branched) and nonylphenol[R]. Luxembourg: Office of Official Journal of the European Communities, 2002.
[5]US Environmental Protection Agency. Screening-level hazard characterization: akylphenols category[R/OL]. 2009 [2017-09-22]. https://www.epa.gov/chemicals-under-tsca.
[6]Canadian Environmental Protection Act, Priority substances list assessment report. Nonylphenol and its ethoxylates[R]. Canada: Environment Canada and Health Canada,1999.
[7]NIU Y M, ZHANG J, DUAN H J, et al. Bisphenol A and nonylphenol in foodstuffs: Chinese dietary exposure from the 2007 total diet study and infant health risk from formulas[J]. Food Chem, 2015,167(6): 320-325.
[8]KLIMISCH H J, ANDREAE M, TILLMANN U. A systematic approach for evaluating the quality of experimental toxicological and ecotoxicological data[J]. Regul Toxicol Pharmacol, 1997, 25(1):1-5.
[9]US Environmental Protection Agency. A review of the reference dose and reference concentration processes[J/OL]. 2013 [2017-09-22]. https://www.epa.gov/osa/basic-information-about-risk-assessment-guidelines-development.
[10]European Commission. European Union risk assessment report (version for TMIII98) [R]. 1998.
[11]BEROL KEMI A B. Nonylphenol acute oral toxicity in rats[R]. Inveresk Research International Project No. 230086, report No. 2379, 1982.
[12]ICI Central Toxicology Laboratory. Nonylphenol (ex-oil Works and Rohm and Haas): comparison of acuteoral toxicities[R]. CTL Report No. CTL/L/708, 1984.
[13]WOO G H, SHIBUTANI M, ICHIKI T, et al. A repeated 28-day oral dose toxicity study of nonylphenol in rats, based on the ‘enhanced OECD test guideline 407’ for screening of endocrine-disrupting chemicals[J].Arch Toxicol, 2007, 81(2):77-88.
[14]HLS A G. Nonylphenol: 28 day oral (dietary) sub-acute toxicity study in the rat[R]. Hazleton UK report no.5917-671/1, 1989.
[15]CUNNY H C, MAYES B A, ROSICA K A, et al. Subchronic toxicity (90-day) study with para-nonylphenol in rats[J]. Reg Toxicol Pharmacol, 1997, 26(2):172-178.
[16]Initiative Umweltrelevante Altstoffe. Teratogenicity study in Wistar rats treated orally with “nonylphenol”[R]. IBR Project No.20-04-0502/00-91, 1992.
[17]NTP. Nonylphenol: multigenerational reproductive effects in Sprague-Dawley rats when exposed to nonylphenol in the diet[R]. R.O.W. Sciences Study No.8989-30, 1997.
[18]DE JAGER C, BORNMAN M S, VAN DER HORST G. The effect of p-nonylphenol, an environmental toxicant with oestrogenic properties, on fertility potential in adult male rats[J]. Andrologia, 1999, 31(2): 99-106.
[19]ROUTLEDGE E J,SUMPTER J P. Structural features of alkylphenolic chemicals associated with estrogenic activity[J]. J Biol Chem,1997, 272(6): 3280-3288.
[20]SOTO A M, JUSTICIA H, WRAY W W, et al. p-Nonyl-phenol: an estrogenic xenobiotic released from “modified” polystyrene[J]. Environ Health Perspect, 1991(92):167-173.
[21]WHITE R, JOBLING S, HOARE S A, et al. Environmentally persistent alkylphenolic compounds are estrogenic[J]. Endocrinology,1994, 135(1):175-182.
[22]ODUM J, LEFEVRE P A, TITTENSOR S, et al. The rodent uterotrophic assay: critical protocol features, studies with nonylphenols, and comparison with a yeast estrogenicity assay[J]. Reg Toxicol Pharmacol,1997, 25(2): 176-188.
[23]LEE P C, LEE W. In vivo estrogenic action of nonylphenol in immature female rats[J]. Bull Environ Contam Toxicol,1996, 57(3): 341-348.
[24]NEGISHI T, KAWASAKI K, SUZAKI S, et al. Behavioral alterations in response to fear-provoking stimuli and tranylcypromine induced by perinatal exposure to bisphenol A and nonylphenol in male rats[J]. Environ Health Perspect, 2004,112(11): 1159-1164.
[25]SHIMIZU H, SUZUKI Y, TAKEMURA N, et al. The results of microbial mutation test for forty-three industrial chemicals[J]. Sangyo Igaku, 1985, 27(6): 400-419.
[26]HLS A G. In vitro mammalian cell gene mutation test with nonylphenol[R]. IBR Project No.95-86-0449-90,1990.
[27]HLS A G. Mutagenittsuntersuchung von nonylphenol im mikrokern-test[R]. Hüls Report Dated 16.08.88, 1988.
[28]HLS A G. In vivo mouse micronucleus test[R]. Hüls Report No. MK-99/0255,1996.
 陈锦瑶,刘兆平,霍娇,岳茜岚,包汇慧,张立实.壬基酚每日可耐受摄入量建议值的探讨[J].中国食品卫生杂志,2018,30(1):104-108.
陈锦瑶,刘兆平,霍娇,岳茜岚,包汇慧,张立实.壬基酚每日可耐受摄入量建议值的探讨[J].中国食品卫生杂志,2018,30(1):104-108.